《AM》贺超良、陈学思院士:两性离子水凝胶包MOF胶囊,pH 响应自分解,用于高效口服 Exendin-4 递送
摘要
口服肽或蛋白质递送被认为是日常皮下注射的革命性替代方案;然而,在胃肠道环境和由粘液和上皮细胞层组成的肠上皮的障碍方面仍然存在重大挑战,导致生物利用度低。
为了防止胃肠道降解并促进穿过肠粘膜的渗透,中国科学院长春应用化学研究所贺超良研究员、陈学思院士团队设计了一种封装两性离子水凝胶涂层金属有机框架 (MOF) 纳米颗粒的 pH 触发自解包胶囊。MOF 纳米粒子具有高 exendin-4 负载能力,两性离子水凝胶层赋予独特的渗透能力,通过粘液层和上皮细胞对纳米载体的有效内化。除了耐胃功能外,由于大量二氧化碳气泡的快速产生,pH 响应胶囊在肠道环境中急剧分离,从而触发纳米颗粒的突然释放。将载有 Exendin-4 纳米颗粒的胶囊口服给药到糖尿病大鼠模型中后,血浆 Exendin-4 水平显着提高超过 8 小时,导致内源性胰岛素分泌显着增加和显着的降血糖作用,具有相对药理学可用性17.3%。由于低血糖风险低,这种口服 exendin-4 策略将为日常和简便的糖尿病治疗提供巨大的潜力。相关论文以题为A pH-Triggered Self-Unpacking Capsule Containing Zwitterionic Hydrogel-Coated MOF Nanoparticles for Efficient Oral Exendin-4 Delivery发表在《Advanced Materials》上。
主图导读
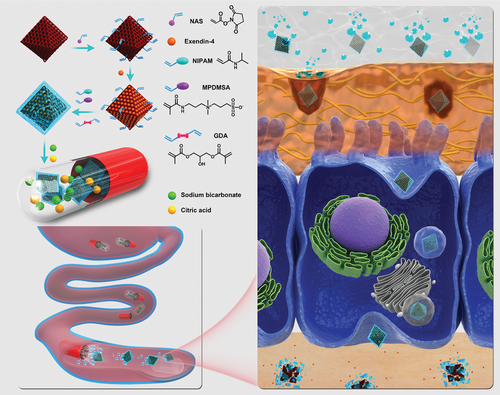
示意图1 含有 Ex@MIL101@Gel± 纳米颗粒用于口服 exendin-4 递送的 pH 触发自解包胶囊的图示。通过丙烯酰改性的 NH2-MIL101纳米粒子、NIPAM 和 MPDMSA 以 GDA 作为交联剂的自由基共聚,获得含有 exendin-4 的水凝胶涂层 MOF 纳米粒子。胶囊保护载有肽的纳米粒子免受胃的酸性环境的影响,并在肠道中解包,产生二氧化碳气泡以促进纳米粒子的运动。纳米颗粒的两性离子表面进一步有助于穿过肠道上皮层的运输。
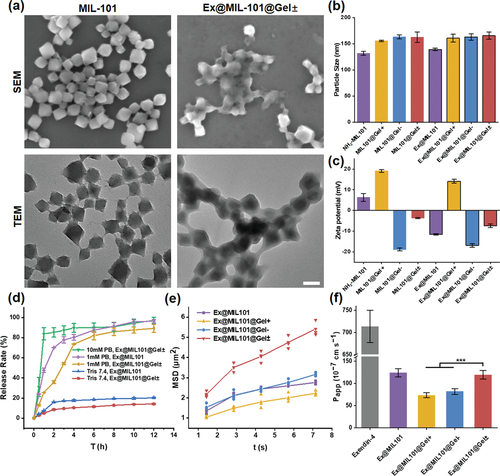
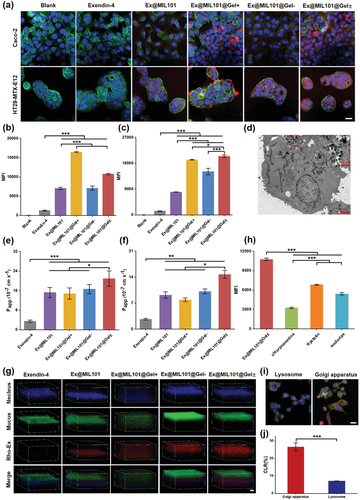
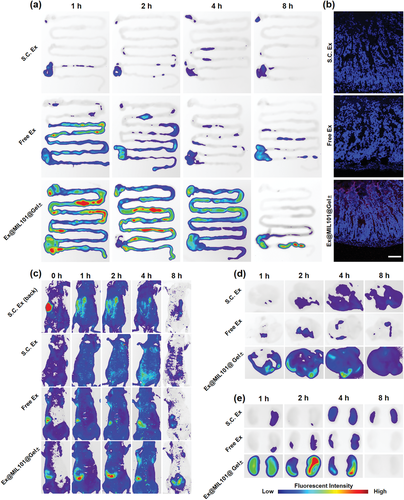

总结
该团队设计并制造了一种含有两性离子 MOF-Gel 纳米颗粒的新型 pH 触发自解包胶囊。pH 响应胶囊在酸性胃环境中保持其完整性,而由于 pH 响应 Eudragit L100-55 涂层的溶解和碳酸氢钠和柠檬酸之间随后的气泡生成反应,它们在中性肠液中被解包。产生的气泡促进了粘液溶液中纳米颗粒的运输。
此外,MOF-Gel 纳米颗粒显示出超过 40% 的高 exendin-4 负载含量,并且肽在含有磷酸盐的溶液中快速释放。与没有水凝胶壳或带单电荷水凝胶壳的 MOF 纳米颗粒相比,具有两性离子水凝胶壳的 MOF 纳米颗粒显示出增强的粘液渗透和 Caco-2 和 E12 细胞的细胞内化。基于荧光成像,在空肠注射到 BALB/c 裸鼠后,含有罗丹明 B 标记的 exendin-4 的 Ex@MIL101@Gel± 纳米颗粒与游离的 exendin-4 相比表现出增强的肠道 exendin-4 吸收。此外,Au@MIL101@Gel±@Cap 的口服给药进一步证实了口服给药的 MOF-Gel 纳米颗粒的有效肠道吸收。在糖尿病大鼠模型中口服给药后,Ex@MIL101@Gel±@Cap 导致血浆 exendin-4 水平显着升高,有效刺激内源性胰岛素分泌,对糖尿病大鼠产生显着的降血糖作用,具有显着的降血糖作用。相对药理利用率为 17.26%。与口服胰岛素治疗相比,使用 exendin-4 发生低血糖的风险较低。包括水凝胶包覆的MOF纳米颗粒和pH响应胶囊在内的载体材料可以轻松获得,高DLE和exendin-4显着增强的口服利用度促进了成本节约,同时为糖尿病患者提供了极大的便利和依从性优势.因此,含有两性离子水凝胶包被的 MOF 纳米颗粒的肠道环境触发的自解包胶囊作为载体具有巨大的潜力,可以克服口服肽递送以有效治疗糖尿病的关键障碍。
| 温馨提示:苏州北科纳米供应产品仅用于科研,不能用于人体,不同批次产品规格性能有差异。网站部分文献案例图片源自互联网,图片仅供参考,请以实物为主,如有侵权请联系我们立即删除。 |
下一篇: 纳米医学产品1


